α―アミノ酸の分子間で、アミノ基とカルボキシル基が脱水縮合して生成した
化合物をペプチドという。ペプチドの一方の末端にはアミノ基が存在し、他方
の末端にはカルボキシル基が存在する。これをそれぞれペプチドのN末端、お
よびC末端とよぶ。N末端のα―アミノ酸のアミノ基は無水酢酸と反応してア
セチル化される性質を持つ。
ペプチドには、タンパク質と同様に固有の生理機能をもつものが多く存在す
る。たとえば、脳で分泌されるメチオニンエンケファリンは、α―アミノ酸5
個から構成される鎖状のペプチドで、モルヒネと同様の鎮痛作用を示す神経伝
達物質である。メチオニンエンケファリンのN末端、C末端いずれかのαアミ
ノ酸はチロシンであることがわかっている。メチオニンエンケファリンの構造
を決定するため、以下の実験を行った。
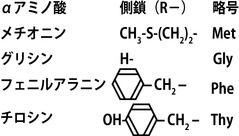
(実験1)メチオニンエンケファリンを
完全に加水分解すると下に示す4種類の
α―アミノ酸が得られた
(実験2)酵素とは、特定の物質の、特定
の反応に対してだけ作用するタンパク質の
触媒のことである。たとえば、キモトリプ
シンという酵素は、芳香族アミノ酸のカルボキシル基側のペプチド結合を特異
的に加水分解する作用をもつ。メチオニンエンケファリンを無水酢酸と反応さ
せてアセチル化した後、キモトリプシンで処理したところ、アセチル化したα
―アミノ酸A、アセチル化していないαーアミノ酸B、および1種類のトリペプチドCが得られた。
(実験3)トリペプチドCには、4つの異なる原子または原子団が結合する炭
素原子が1つだけ存在した。
(実験4)α―アミノ酸Bに濃硝酸を加えて加熱しても、黄変しなかった。
問1 実験3の結果から、トリペプチドCには、あるα―アミノ酸が複数含ま
れていることがわかる。この複数個含まれているα―アミノ酸の名前と数を、
その理由とともに60字以内で答えよ。
問2 α―アミノ酸Aの名前を書け。
問3 一連の実験結果から予想されるメチオニンエンケファリンの構造を、以
下の例にならって略号を使ってかけ。N末端のα―アミノ酸が左端に、C末端
のα―アミノ酸が右端になるようにかけ。
例 Met―Gly―Phe―Tyr―Met
↓
↓
↓
(考える)
↓
↓
↓
答
問1 α―アミノ酸の名称 グリシン 数 2
トリペプチドC内には不斉炭素原子が1個あるので、残りの構成アミノ酸は
不斉炭素原子をもたないグリシンである。
問2 α―アミノ酸の名称 チロシン
問3 Thy―Gly―Gly―Phe―Met
解説
問3
1、前文「メチオニンエンケファリンのN末端、C末端いずれかのαアミ
ノ酸はチロシンであることがわかっている。」
より
Thy-●ー●ー●ー●
あるいは
●ー●ー●ー●ーThy
2、「芳香族アミノ酸(PheかThyのカルボキシル基側のペプチド結合を特異
的に加水分解する作用をもつ」ので
a,
芳|芳|●ー●ー●
か
b,
芳|●ー●ー芳|●
の場合にのみ
1・3・1に分離できる
(「芳」は「芳香族アミノ酸を示し、|はそのカルボキシ側の切断箇所を示す。
よって1の可能性の中で
Thy-●ー●ー●ー●
のみが正しいとわかる。
すると芳香族アミノ酸の消去法で
Thy|●ー●ーPhe|●
とわかる。
3、実験3の情報から
Thy|Gly-Gly-Phe|●
とわかる。
4消去法で
Thy|Gly-Gly-Phe|Met
と決定できる。
また
実験4からアミノ酸Bは芳香族アミノ酸ではないとわかる。
(濃硝酸を加えると黄変する「キサントプロテイン反応は芳香族アミノ酸におきる)
すると
切断は
A(Thy)|C(トリペプチド)|B(Met)
とわかり、
「メチオニンエンケファリンを無水酢酸と反応さ
せてアセチル化した後、キモトリプシンで処理したところ、アセチル化したα
―アミノ酸A」が生じるとあるが、アセチル化(酢酸CH3COOHとアミノ基NH2で脱水縮合が起こりCH3CONHとなる)はアミノ基末端におきるという事実とも一致する。
なお「アセチル化」についてはまた別の角度で述べます。
またこのように3〜8アミノ酸のペプチドの構造を決定する問題が化学ではよく出されます。上記のように順に解くのが原則